कीटोन
द्वितीयक अल्कोहल के बी विहाइड्रोजनीकृत उत्पाद को कीटोन (ketones in Hindi) कहते हैं। कीटोन में कार्बनिक समूह >C=O होता है।
कीटोन बनाने की विधि
1. एल्कोहाॅल से – द्वितीय ऐल्कोहाॅल के ऑक्सीकरण द्वारा कीटोन प्राप्त किया जाता है।
\scriptsize \begin{array}{rcl} RCHOHR’ \\ 2°\,एल्कोहाॅल \end{array} \xrightarrow [K_2Cr_2O_7/H_2SO_4] {[O]} \scriptsize \begin{array}{rcl} RCOR’ \\ कीटोन \end{array} + H2O
2. बेंजीन से – बेंजीन की निर्जल एल्युमिनियम क्लोराइड की उपस्थिति में अम्ल क्लोराइड के साथ क्रिया कराने पर किटोन प्राप्त होते हैं। इस अभिक्रिया को फ्रिडेल क्राफ्ट्स अभिक्रिया कहते हैं।
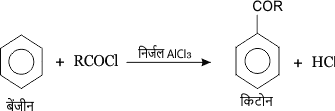
3. वसीय अम्लों से – वसीय अम्लों की वाष्प को 573K ताप पर तप्त MnO प्रवाहित करने पर किटोन बनते हैं।
\scriptsize \begin{array}{rcl} 2RCOOH \\ वसीय\,अम्ल \end{array} \xrightarrow {MnO/573K} \scriptsize \begin{array}{rcl} RCOR \\ कीटोन \end{array} + H2O + CO2 ↑
कीटोन के भौतिक गुण
- कीटोन जिनमें 11 तक कार्बन परमाणु होते हैं वह सभी के किटोन रंगहीन द्रव होते हैं। एवं C11 से अधिक कार्बन परमाणु वाले किटोन ठोस होते हैं।
- सभी कीटोन की गंध फलों जैसी रुचिकर होती है।
- कीटोन का क्वथनांक एल्कोहलों एवं कार्बोक्सिलिक अम्ल से कम होता है। जबकि समान अणु भार वाले ईथर तथा हाइड्रोकार्बन से उच्च होता है।
- कीटोन के निम्न सदस्य जल के साथ हाइड्रोजन बंध बनाते हैं। जिस कारण यह जल में विलेय होते हैं। अणुभार के बढ़ने पर जल में इनकी विलेयता घटती जाती है।
कीटोन के रासायनिक गुण
1. हैलोजनीकरण – एल्किल समूह के हाइड्रोजन परमाणुओं का हैलोजन परमाणुओं द्वारा प्रतिस्थापन हो जाता है। अर्थात किटोन हैलोजनीकरण अभिक्रिया देता है।
CH3COCH3 + 3Cl2 \longrightarrow CCl3COCH3 + 3HCl
2. क्लोरोफॉर्म के साथ अभिक्रिया – कीटोन की पोटैशियम हाइड्रोक्साइड की उपस्थिति में क्लोरोफॉर्म के साथ संघनित होकर क्लोरो हाइड्रोक्सी यौगिक बनाते हैं।

3. सल्फोनीकरण – कीटोन की सांद्र H2SO4 के साथ क्रिया करने पर सल्फोनीकरण हो जाते हैं।
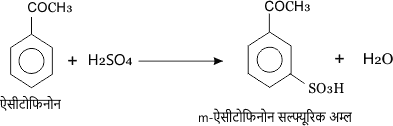
कीटोन के उपयोग
- एसीटोन का उपयोग एसिटिलीन सैल्यूलोज एसीटेट तथा सेल्यूलोज नाइट्रेट के लिए विलायक के रूप में किया जाता है।
- क्लोरोफॉर्म के निर्माण में भी एसीटोन प्रयोग होता है।
- कृत्रिम इत्र के निर्माण में।
- एसीटोन तथा एथिल मेथिल किटोन औद्योगिक में विलायक के रूप में प्रयोग होते हैं।